SEMANA
|
MES
|
TEMAS Y SUBTEMAS
| ||||||||||||||||||||||||||||||||||
15-20
|
FEBRERO
|
Repaso
| ||||||||||||||||||||||||||||||||||
22-27
|
FEBRERO
|
Repaso
| ||||||||||||||||||||||||||||||||||
29-5
|
FEBRERO/MARZO
|
Repaso
| ||||||||||||||||||||||||||||||||||
7-12
|
MARZO
|
Medición de la Temperatura
 Se han inventado muchos instrumentos para medir la temperatura de forma precisa. Todo empezó con el establecimiento de una escala de temperaturas. Esta escala permite asignar un número a cada medida de la temperatura. Se han inventado muchos instrumentos para medir la temperatura de forma precisa. Todo empezó con el establecimiento de una escala de temperaturas. Esta escala permite asignar un número a cada medida de la temperatura.
A principios del siglo XVIII, Gabriel Fahrenheit (1686-1736) creó la escala Fahrenheit. Fahrenheit asignó al punto de congelación del agua una temperatura de 32 grados y al punto de ebullición una de 212 grados. Su escala está anclada en estos dos puntos.
Unos años más tarde, en 1743, Anders Celsius (1701-1744) inventó la escala Celsius. Usando los mismos puntos de anclaje Celsius asignó al punto de congelación del agua una temperatura de 0 grados y al de ebullición una de 100 grados. La escala Celsius se conoce como el Sistema Universal. Es el que se usa en la mayoría de los paises y en todas las aplicaciones científicas.
Hay un límite a la temperatura mínima que un objeto puede tener. La escala Kelvin está diseñada de forma que este límite es la temperatura 0. La relación entre las diferentes escalas de temperatura es la siguiente:
Para ir de una escala a otra puede usar esta calculadora para convertir temperaturas(Inglés).
A la temperatura del cero absoluto no hay movimiento y no hay calor. Es cuando todo el movimiento atómico y molecular se detiene y es la temperatura más baja posible. El cero absoluto tiene lugar a 0 grados Kelvin, -273.15 grados Celsius o -460 grados Farenheit. Todos los objetos tienen una temperatura más alta que el cero absoluto y por lo tanto emiten energía térmica o calor.
Si queremos entender qué significa la temperatura a nivel molecular debemos recordar que la temperatura es la energía media de las moléculas que componen una sustancia. Los átomos y las moléculas no siempre se mueven a la misma velocidad. Esto significa que hay un rango de energías entre ellas. En un gas, por ejemplo, las moléculas se mueven en direcciones aleatorias y a diferentes velocidades - algunas se mueven rápido y otras más lentamente. A veces estas moléculas colisionan entre si. Cuando esto tiene lugar las moléculas que se mueven más deprisa transfieren parte de su energía a las que se mueven más despacio, haciendo que la más rápidas se ralenticen y las más lentas se aceleren. Si ponemos más energía en el sistema, la velocidad media de las moléculas se incrementa, lo que hace que se produzca energía térmica o calor. Por lo tanto, temperaturas altas corresponden a sustancias que tienen un movimiento medio molecular mayor. Nostros, por supuesto, no podemos sentir ni medir el movimiento de cada molécula, solo el movimiento medio de todas ellas.
Pulse aquí para ver un "applet" de java que muestra cómo las moléculas se mueven a diferentes temperaturas (Inglés).
En un objeto frío las moléculas se mueven lentamente y en uno caliente se mueven deprisa. Cuando dos objetos se ponen en contacto sus movimientos moleculares medios se igualan y cuando esto ocurre se dice que han alcanzado equilibrio térmico.
Para más información sobre la temperatura vea:
Hay también varios sitios en la red donde se discuten diferentes instrumentos para medir la temperatura y cómo funciona cada uno
| ||||||||||||||||||||||||||||||||||
14-19
|
MARZO
|
Diferencia entre Calor y Temperatura
Todos sabemos que cuando calentamos un objeto su temperatura aumenta. Amenudo pensamos que calor y temperatura son lo mismo. Sin embargo este no es el caso. El calor y la temperatura están relacionadas entre si, pero son conceptos diferentes.
El calor es la energía total del movimiento molecular en una sustancia, mientras temperatura es una medida de la energía molecular media. El calor depende de la velocidad de las partículas, su número, su tamaño y su tipo. La temperatura no depende del tamaño, del número o del tipo. Por ejemplo, la temperatura de un vaso pequeño de agua puede ser la misma que la temperatura de un cubo de agua, pero el cubo tiene más calor porque tiene más agua y por lo tanto más energía térmica total.
El calor es lo que hace que la temperatura aumente o disminuya. Si añadimos calor, la temperatura aumenta. Si quitamos calor, la temperatura disminuye. Las temperaturas más altas tienen lugar cuando las moléculas se están moviendo, vibrando y rotando con mayor energía.
Si tomamos dos objetos que tienen la misma temperatura y los ponemos en contacto, no habrá transferencia de energía entre ellos porque la energía media de las partículas en cada objeto es la misma. Pero si la temperatura de uno de los objetos es más ala que la otra, habrá una transferencia de energía del objeto más caliente al objeto más frío hasta que los dos objetos alcancen la misma temperatura.
La temperatura no es energía sino una medida de ella, sin embargo el calor sí es energía
| ||||||||||||||||||||||||||||||||||
22-26
|
MARZO
|
Transferencia de Calor
Calor
2.1 CONCEPTOS PREVIOS
En el S.I. tenemos la caloría (cal), que se define como la cantidad de transferencia de energía necesaria para elevar la temperatura de 1 g de agua de 14,5 °C a 15,5 °C.
 (1) (1)
La unidad de energía en el sistema convencional en E.E.U.U. es la unidad térmica británica (Btu), que se define como la cantidad de transferencia de energía necesaria para elevar la temperatura de 1 lb de agua de 63 °F a 64 °F.
2.2 CAPACIDAD CALORÍFICA (C)
La capacidad calorífica C de una muestra particular de una sustancia se define como la cantidad de energía necesaria para elevar en 1 °C la temperatura de la muestra. De esta definición vemos que si la energía Q se produce un cambio ?T en la temperatura de una muestra, entonces
 (2) (2)
2.3 CALOR ESPECÍFICO (c)
El calor específico c de una sustancia es la capacidad calorífica por unidad de masa. Por lo tanto, si la energía Q se transfiere a una muestra de una sustancia con masa m y la temperatura de la muestra cambia en ?T, entonces el calor específico de la sustancia es
 (3) (3)
El calor específico es en esencia una medida de lo térmicamente insensible que es una sustancia a la suma de energía. Cuanto mayor es el calor especifico de un material, más energía debe agregarse a una masa del material para causar un cambio particular de temperatura. La tabla 1 indica calores específicos representativos.
De esta definición, podemos relacionar la energía Q transferida entre una muestra de masa m de un material y su entorno a un cambio de la temperatura ?T como
 (4) (4)
Tabla 1

2.4 CONSERVACIÓN DE LA ENERGÍA: CALORIMETRÍA
Una técnica para medir calor específico comprende en calentar una muestra a una temperatura conocida Tx poniéndola en un vaso que contenga agua de masa conocida y temperatura Tw < Tx y midiendo la temperatura del agua después de alcanzar el equilibrio. Esta técnica se denomina calorimetría, y los dispositivos en los que se presenta esta transferencia de energía se llaman calorímetros. Si el sistema de la muestra y el agua está aislado, la ley de conservación de la energía exige que la cantidad de energía que sale de la muestra (de calor específico desconocido) sea igual a la cantidad de energía que entre al agua.
La conservación de la energía nos permite escribir la representación matemática de este enunciado de energía como
 (5) (5)
El signo negativo de la ecuación es necesario para mantener consistencia con nuestra convención de signos para calor.
 Cambio de fase y calor latente
Es frecuente que una sustancia experimente un cambio de temperatura cuando se transfieres energía entre ella y su entorno. Hay situaciones, sin embargo, en las que la transferencia de energía no resulta en un cambio de temperatura. Éste es el caso siempre que las características físicas de la sustancia cambien de una forma a la otra; a este cambio se conoce comúnmente como cambio de fase. Dos cambios de fase comunes son de solido a líquido (fusión) y de líquido a gas (ebullición). Todos estos cambios de fase corresponden a un cambio en energía interna, pero ningún cambio en temperatura.
La cantidad de energía transferida durante un cambio de fase depende de la cantidad de sustancia de que se trate. Si la cantidad Q de transferencia de energía se necesita para cambiar de fase de una masa m de una sustancia, la razón L=Q/m caracteriza una importante propiedad térmica de esa sustancia. Debido a que esta energía agregada o eliminada no resulta en un cambio de temperatura, la cantidad L se denomina calor latente ("calor oculto") de la sustancia. El valor de L para una sustancia depende se la naturaleza del cambio de fase, así como de las propiedades de la sustancia.
De la definición de calor latente, y de nuevo seleccionando el calor como nuestro mecanismo de transferencia de energía, encontramos que la energía necesaria para cambiar la fase de una masa m dada se una sustancia pura es
 Transferencia de calor
El calor se transfiere, o se transmite, de cosas más calientes a cosas más frías. Si están en contacto varios objetos con temperaturas distintas, los que están más calientes se enfrían y los que están más fríos se calientan. Tienden a alcanzar una temperatura común. Esta igualación de temperaturas se lleva a cabo de tres maneras: por conducción, convección y radiación.

Figura 1. Esquema de los mecanismos de transferencia de calor
La conducción es el mecanismo de transferencia de calor en escala atómica a través de la materia por actividad molecular, por el choque de unas moléculas con otras, donde las partículas más energéticas le entregan energía a las menos energéticas, produciéndose un flujo de calor desde las temperaturas más altas a las más bajas. Los mejores conductores de calor son los metales. El aire es un mal conductor del calor. Los objetos malos conductores como el aire o plásticos se llaman aislantes.

Donde k (en Watt/m. K) se llama conductividad térmica del material, magnitud que representa la capacidad con la cual la sustancia conduce calor y produce la consiguiente variación de temperatura; y dT/dx es el gradiente de temperatura. El signo menos indica que la conducción de calor es en la dirección decreciente de la temperatura.

Figura 2.
La convección es el mecanismo de transferencia de calor por movimiento de masa o circulación dentro de la sustancia. Puede ser natural producida solo por las diferencias de densidades de la materia; o forzada, cuando la materia es obligada a moverse de un lugar a otro, por ejemplo el aire con un ventilador o el agua con una bomba. Sólo se produce en líquidos y gases donde los átomos y moléculas son libres de moverse en el medio.
En la naturaleza, la mayor parte del calor ganado por la atmósfera por conducción y radiación cerca de la superficie, es transportado a otras capas o niveles de la atmósfera por convección.
Un modelo de transferencia de calor H por convección, llamado ley de enfriamiento de Newton, es el siguiente:
 (7) (7)
Donde h se llama coeficiente de convección, en Watt/ (m2. K), A es la superficie que entrega calor con una temperatura TA al fluido adyacente, que se encuentra a una temperatura T, como se muestra en el esquema de la figura 3.

Figura 3.
El flujo de calor por convección es positivo (H > 0) si el calor se transfiere desde la superficie de área A al fluido (TA > T) y negativo si el calor se transfiere desde el fluido hacia la superficie (TA < T).
La radiación térmica es energía emitida por la materia que se encuentra a una temperatura dada, se produce directamente desde la fuente hacia afuera en todas las direcciones. Esta energía es producida por los cambios en las configuraciones electrónicas de los átomos o moléculas constitutivos y transportada por ondas electromagnéticas o fotones, por lo recibe el nombre de radiación electromagnética. La masa en reposo de un fotón (que significa luz) es idénticamente nula. Por lo tanto, atendiendo a relatividad especial, un fotón viaja a la velocidad de la luz y no se puede mantener en reposo. (La trayectoria descrita por un fotón se llama rayo). La radiación electromagnética es una combinación de campos eléctricos y magnéticos oscilantes y perpendiculares entre sí, que se propagan a través del espacio transportando energía de un lugar a otro.
A diferencia de la conducción y la convección, o de otros tipos de onda, como el sonido, que necesitan un medio material para propagarse, la radiación electromagnética es independiente de la materia para su propagación, de hecho, la transferencia de energía por radiación es más efectiva en el vacío. Sin embargo, la velocidad, intensidad y dirección de su flujo de energía se ven influidos por la presencia de materia. Así, estas ondas pueden atravesar el espacio interplanetario e interestelar y llegar a la Tierra desde el Sol y las estrellas. La longitud de onda (?) y la frecuencia (?) de las ondas electromagnéticas, relacionadas mediante la expresión
Los fotones son emitidos o absorbidos por la materia. La longitud de onda de la radiación está relacionada con la energía de los fotones, por una ecuación desarrollada por Planck:
 (8) (8)
Donde h se llama constante de Planck, su valor es h = 6,63 x 10-34 Joule. Seg.
Fuente
Capítulo 20: El calor y la primera ley de termodinámica
Leer más: http://www.monografias.com/trabajos88/calor-conceptos-y-tipos-transferencia-calor/calor-conceptos-y-tipos-transferencia-calor.shtml#ixzz448VqXzH3 | ||||||||||||||||||||||||||||||||||
28-2
|
MARZO-ABRIL
|
Efecto de calor sobre los cuerpos
Efectos del calor sobre los cuerpos
Aparte del lógico aumento de la temperatura en los cuerpos, cuando se calienta un cuerpo pueden producirse otra serie de efectos, entre los que destacan dos:
1) Cambios de estado
Al comunicar energía a una sustancia, según la teoría cinética de la materia aumenta la energía cinética de sus partículas, de forma que comienzan a moverse más rápidamente, siendo más probable que adquieran la energía necesaria como para vencer las fuerzas que las mantienen unidas, cambiando su configuración.
Cuando se calienta un sólido, las partículas que se encuentran en posiciones prácticamente fijas comienzan a vibrar con mayor amplitud y velocidad, hasta que se funde. Al alcanzar el punto de energía cinética máxima, la energía adicional se emplea en vencer las fuerzas que mantienen las partículas unidas entre sí, abandonando sus posiciones y pasando al estado líquido.
En este proceso de cambio de estado se produce un intercambio de calor, positivo en el caso de paso de sólido a líquido y negativo pero de igual valor que el anterior en el paso de líquido a sólido, que se utiliza en romper las uniones que mantienen unidas las partículas:
Se denomina calor latente (L) a la energía intercambiada para producir el cambio de estado de un kilogramo de materia. A temperatura constante (temperatura de cambio de estado):

El calor latente se mide en J/kg.
Observa la imagen, en la que se representa la variación de temperatura producida al comunicar la misma cantidad de calor a la misma masa de tres sustancias diferentes: hielo, alcohol y mercurio.
¿Qué tienen en común las tres sustancias? Cuando comienza a producirse el cambio de estado, la gráfica de la temperatura frente al tiempo es una recta horizontal, es decir, la temperatura no cambia durante un cambio de estado.
Esto ocurre porque la energía se utiliza para romper los enlaces entre partículas en vez de en incrementar la temperatura del sistema: mientras se produce un cambio de estado la temperatura del cuerpo permanece constante.
La explicación en los restantes cambios de estado según la teoría cinética es similar a la que se ha dado para el caso de sólido a líquido. Esta existencia de distintos cambios de estado implica la existencia de distintos calores latentes: calor latente de fusión (Lf), calor latente de vaporización (Lv) y calor latente de sublimación (Ls)
Colocamos sobre un plato un cubito de hielo de 50 g que se encuentra inicialmente a una temperatura de -15 ºC. Al cabo de unas horas volvemos y encontramos que se ha transformado en agua que se encuentra a temperatura ambiente (25 ºC).
¿Qué energía se ha suministrado al hielo para efectuar esta transformación?
Datos: ce_hielo = 2100 J/(kg·K), ce_agua = 4180 J/(kg·K), Lfusión = 3.34·105 J/kg
Calcula la energía necesaria para evaporar totalmente 100 g de agua a 90 ºC.
Datos: ce_agua = 4180 J/(kg·K), Levaporación = 2.26·106 J/kg
2) Dilatación térmica
Al aumentar la energía cinética de las partículas, aumenta su movilidad lo que lleva asociado un incremento del tamaño del cuerpo; a este fenómeno se le denominadilatación.
La dilatación se produce en todos los estados de la materia:
En ingeniería es muy importante tener en cuenta los efectos de la dilatación a la hora de construir edificios o carreteras. De hecho, si observas cualquier viaducto suficientemente largo, observarás cómo, cada cierta distancia, existen unas separaciones entre los bloques de asfalto, similares a las que se ven en la imagen. A estos dispositivos se les denominajuntas de dilatación y se instalan precisamente para que los efectos de ésta no dañen la estructura del puente. Algo similar ocurre con los raíles en las vías de los trenes.
En las montañas rusas también hay juntas de dilatación, para conseguir que no se compriman al dilatarse con las altas temperaturas del verano, y por efecto del calor desprendido por el rozamiento de las vagonetas cuando se mueven.
Una barra de acero tiene una longitud de 100 m medida a 20 ºC. Al calentarla hasta 50 ºC se encuentra que su longitud ha aumentado en 3.6 cm. ¿Cuál es el coeficiente de dilatación α del acero?
Dilatación anómala del agua
El agua, a diferencia de la mayor parte de sustancias, disminuye de volumen con el aumento de temperatura en el intervalo entre 0 ºC y 4 ºC . Dicho en otras palabras, en este intervalo el coeficiente de dilatación del agua es negativo. Lo mismo ocurre cuando se congela.
Este comportamiento es fundamental en la vida en la Tierra, ya que cuando un lago se enfría, el agua fría de la superficie desciende al fondo por su mayor densidad; ahora bien, cuando la temperatura llega a los 4 ºC este movimiento cesa. Además, como el hielo es menos denso que el agua, flota y actúa como aislante evitando que siga perdiéndose calor. Esto provoca que los lagos se congelen más fácilmente y permite que los seres vivos que soportan bien el agua fría pero no el hielo continúen con vida. Este hecho fue básico durante las glaciaciones para evitar la extinción de numerosas especies.
| ||||||||||||||||||||||||||||||||||
4-9
|
ABRIL
|
Cuerpos Solidos
DEFINICIÓN DESÓLIDO
Sólido, del latín solĭdus, es algo fuerte, macizo o firme. Por ejemplo: “Necesito una madera sólida para construir una mesa donde pueda apoyar el televisor nuevo”, “Ayer fui a ver una casa, pero no me gustó ya que no parecía muy sólida”, “Tengo que comprar una plancha de cartón sólido para que mi hijo lleve a la escuela”.
No obstante, no hay que olvidar tampoco que sólido es una palabra que también se utiliza en el ámbito histórico. En concreto, la misma se usa para hacer referencia a una moneda que usaban los romanos y que equivalía a lo que eran 25 dinarios de oro.
Los cuerpos sólidos, por otra parte, son aquellos que mantienen forma y volumen constantes gracias a la gran cohesión de sus moléculas. La fase sólida es uno de los cuatro estados de agregación de la materia, junto al líquido, el gaseoso y el plasmático.
Es interesante conocer que existen varias disciplinas que se encargan precisamente de estudiar y analizar en profundidad los sólidos. En concreto entre las mismas está la ciencia de los materiales, la física del estado sólido o la química.
Entre las propiedades de los sólidos, se destacan la elasticidad (un sólido puede recuperar su forma original cuando es deformado), la dureza (no puede ser rayado por otro cuerpo más blanco) y la fragilidad (los sólidos pueden romperse en muchos pedazos ya que son quebradizos).
A todas estas características o propiedades de los sólidos habría que añadir también la resistencia que presentan a modificar lo que sería su posición en estado de reposo, la ductilidad, la tenacidad y la maleabilidad.
A baja temperatura y presión constante, los cuerpos sólidos forman generalmente estructuras cristalinas. Esto les permite soportar fuerzas sin deformarse en apariencia. Los sólidos suelen gozar de forma y volumen definidos (a diferencia de los líquidos o los gases) y tienen alta densidad (sus moléculas están muy cerca).
Un ejemplo de estado sólido es el hielo (agua congelada). Esta misma sustancia, formada por dos átomos de hidrógeno y uno de oxígeno, puede encontrarse en estado líquido (en los océanos) o en estado gaseoso (el vapor).
Es irremediable que cuando hablemos de sólidos se nos vengan a la materia los líquidos. Y es que, podríamos decir, se han convertido en nuestro acervo cultural en antónimos, en opuestos.
Lee todo en: Definición de sólido - Qué es, Significado y Concepto http://definicion.de/solido/#ixzz448WfKEud | ||||||||||||||||||||||||||||||||||
11-16
|
ABRIL
|
Relación entre la fuerza,área y presión en los fluidos
Es la relación entre una fuerza aplicada y el área sobre la cual actúa. Presión = fuerza (en newton)/superficie (m²). La unidad se llama Pascal = 1 N/m²
Al medir presiones elevadas, como gases que están comprimidos o vapor de una caldera, se usa la unidad denominada atmósfera (atm) 1atm = 1.013 x 105 N/m²
ejemplo:
Un elefante que pesa 40000 N (4000 kg) se mantiene sobre una pata con un área de 1000 cm2 (1/10 m2). La presión que ejerce es: P = 40000/1/10 = 40000 N/m2
¿Cuál es la presión que ejerce una mujer de 400 N (40 kg) sobre un tacón de aguja de área 1cm2 (1/10000 m2)? P = 400 /1/10000 = 4000000 N/m2
Resultado = 10 veces mayor que la presión que ejerce el elefante.
La hidrostática es la parte de la física que se ocupa de estudiar los fluidos líquidos en reposo.
Presión hidrostática Es la presión que se ejerce en un punto a una profundidad determinada
Los líquidos y los gases ejercen ejercen fuerzas perpendiculares a las paredes del recipiente, pero también el fondo del mismo recibe mayor presión al tener que soportar las capas que están arriba formando columnas imaginarias.
Ejemplo:
¿Cual es la presión que recibe un cuerpo sumergido en el agua de una alberca que se encuentra a 2m de profundidad?

PRINCIPIO DE PASCAL
La presión ejercida en cualquier lugar de un líquido contenido en un recipiente cerrado, se transmite, sin disminuir, por todo el líquido y actúa en ángulo recto con respecto a todas las superficies del recipiente.
Aplicaciones:
Ejemplo:

Todo cuerpo que es total o parcialmente sumergido en un líquido es empujado hacia arriba con una fuerza igual en magnitud al peso del volúmen del líquido que desaloja.
Aplicaciones:
ejemplo:
E = 13.6 x 2 Kgf o E = 27.2 Kgf = 272 N
Daniel Bernoulli estudió el comportamiento de los fluidos en movimiento que afirma que la suma de la presión y las energías cinética y potencial del líquido es constante.
Demostró que cuando aumenta la velocidad de un fluido (aire, agua, aceite...) su presión disminuye
Esta es una de las principales razones por las que vuelan los aviones. La forma que tiene un ala de avión, permite que el aire circule más rápido por la parte superior del ala y más lento por su parte inferior Si aplicamos el Principio de Bernoulli, observamos que la presión bajo el ala es mayor que encima de ella y, por lo tanto, el avión recibe un empujón hacia arriba. Cuando el avión se mueve debido a la fuerza del motor, el aire circula por sus alas produciendo el empuje que lo hace volar.
TENSION SUPERFICIAL

Es la acción de las fuerzas que se presentan por la atracción entre las moléculas del líquido. Los jabones y detergentes disminuyen la tensión superficial por lo que se les denomina sustancias tensoactivas.
Un fenómeno relacionado con la tnsión superficial es la capilaridad que es el ascenso de líquidos a través de un tubo muy delgado; y esto se debe a la fuerza de atracción que existe entre las moléculas del agua y la pared interna del tubo, o sea, la fuerza de adhesión. ejemplos : las plantas donde a través de las raíces el agua y los nutrientes suben a la parte más alta.
PRESION ATMOSFERICA
Es la presión ejercida por el peso del aire atmósferico sobre cualquier superficie en contacto con él. Cotidianamente en todo momento encontramos situaciones en que es evidente la existencia de la presión atmósferica.
Aplicaciones de la presión atmósferica
Medida de la presión atmósferica
Variación de la presión atmósferica con la altura
 | ||||||||||||||||||||||||||||||||||
18-23
|
ABRIL
|
Presión entre columnas de líquidos
Presión en columnas de líquidos.
Al introducir una placa de plástico o de cartón, empujada por un tubo, en un recipiente con agua, sentimos resistencia a ser sumergida, pero además la placa no se separa del tubo. Si intentamos empujarla con una vara, notamos que se requiere de cierta fuerza para lograr separarla del tubo. ¿Qué la empuja?, ¿de qué depende ese empuje? Tal vez notemos que la fuerza necesaria para separarla será mayor cuanto mayor sea la profundidad; pero si estamos a una misma profundidad, notaremos que la fuerza es la misma.
Como hemos anotado anteriormente, toda la materia está formada por moléculas, que en los líquidos están en movimiento desplazándose en su interior y colisionando constantemente. Así, si imaginamos la región de agua que está justo debajo de la placa, tendremos una gran cantidad de moléculas golpeándola simultáneamente. El resultado de esas colisiones es una fuerza de empuje que se dirige hacia arriba y que debe superarse para separar la placa del tubo, es decir, moverla hacia abajo (Fig. 1).

Fig. 1 Las colisiones de las moléculas tienen como resultado una fuerza de empuje hacia arriba sobre la placa.
Si ahora introducimos una placa con el doble de área, notaremos que se requiere mayor fuerza para separarla del tubo, lo cual implica que hay más moléculas chocando con la placa. Esto ocurre así siempre en una proporción constante; entre más área, más fuerza de empuje, de manera que:
F = PA
Donde F es la magnitud de la fuerza de empuje, A el área, y P, que en este caso es la constante de proporcionalidad, es la presión.
De hecho, es común que la presión se exprese por la ecuación:
Así, para todo lugar de un fluido a la misma profundidad, la presión será la misma. Esta explicación se aplica al barómetro de Torricelli: las moléculas de la atmósfera ejercen presión sobre el mercurio de la cubeta y mantienen a cierta altura la columna en el tubo cerrado (Fig. 2).

Fig. 2 Al verter agua en el tubo al mismo nivel que el de la cubeta, las presiones son iguales, por lo que la placa se separará fácilmente.
Una forma de separar la placa del tubo sin empujar, consiste en llenarlo con agua; así, al tener la placa encima el mismo nivel de agua, recibirá colisiones tanto por debajo como por arriba, y el resultado neto será una fuerza prácticamente cero (sería cero si el espesor de la placa fuese cero).
Con ello podemos darnos cuenta que la fuerza de empuje es igual a la del peso de la columna de agua, justo encima de la placa, por lo que:
F = mg
en donde m es la masa del líquido y g es la aceleración de la gravedad. Al sustituir se obtiene:

La unidad de presión es N/m2 (newtons/metros cuadrados) en el Sistema Internacional de Unidades, y se le conoce como pascal (Pa). Existen distintos tipos de unidades de la presión; entre las más comunes se encuentran la atmósfera (atm), que equivale a 1.01x105 Pa (este valor corresponde a la presión atmosférica a nivel del mar y se toma como punto de referencia), y los milímetros de mercurio (mm Hg), que equivalen a 1.33x102 Pa.
Para determinar cómo es la relación de la presión con la altura, pensemos en el fondo de un recipiente cuya superficie tiene área A; entonces la presión del líquido en un área estaría dada por el peso del líquido en esa área, es decir: 
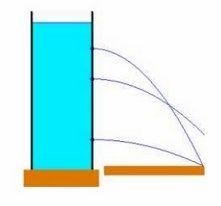
Fig. 3 La presión sólo depende de la profundidad y de la densidad; por eso no importa si el recipiente es delgado o ancho; a la misma profundidad la presión será la misma.
Podemos sustituir la masa m en función del volumen del líquido utilizando la expresión:
que viene de la definición de densidad:
Sustituyendo la ecuación de la presión tenemos que:
Como el volumen de un objeto se puede expresar también como el producto del área de la base por la altura (V = Ah), se encuentra finalmente que:
P = ρAhg / A = ρgh
en donde ρ es la densidad, g es la aceleración de la gravedad y h es la altura de la columna del líquido. Lo mismo ocurre para cualquier lugar del líquido. Lo anterior nos indica que la presión en un área no depende de la cantidad de líquido, sino sólo de su densidad y de la altura de la columna. Por ello, la presión en dos recipientes que tienen distinta área será la misma si la altura de la columna de líquido es la misma.
Blas Pascal (1623-1662) supo de los experimentos de Torricelli y, apoyado por los resultados en la construcción del barómetro, se propuso demostrar que el peso del aire era la causa de su funcionamiento y que, por tanto, cambia al variar la altitud. Pascal repitió el experimento de Torricelli en lo más alto del cerro Puy de Dome, cercano a la ciudad de Clermont, Francia, y en el lugar más bajo de la ciudad; encontró que en el punto más alto la columna de mercurio era menor que en el más bajo, indicando que al haber más aire, éste pesa más y, por tanto, la columna es más alta.
Al aceptar que el barómetro funcionaba debido a la presencia de una columna de aire sobre la superficie del recipiente que contenía mercurio, se pusieron al descubierto dos aspectos: que el vacío podía existir en la naturaleza y que el aire era similar al agua, por lo cual podían aplicarse al aire los conocimientos que se tenían sobre la acción del agua en diversos fenómenos. Torricelli y Pascal utilizaron el concepto de peso del aire sobre la columna de líquido, pues consideraban que este peso empujaba la superficie del líquido fuera del tubo, pero no llegaron a establecer el concepto de presión. | ||||||||||||||||||||||||||||||||||
25-30
|
ABRIL
|
Propiedades de los Fluidos
| |||||||||||||||||||||
2-7
|
MAYO
|
Tensión y superficie
TENSIÓN SUPERFICIAL:
Las moléculas de un líquido se atraen entre sí, de ahí que el líquido esté "cohesionado". Cuando hay una superficie, las moléculas que están justo debajo de la superficie sienten fuerzas hacia los lados, horizontalmente, y hacia abajo, pero no hacia arriba, porque no hay moléculas encima de la superficie. El resultado es que las moléculas que se encuentran en la superficie son atraídas hacia el interior de éste. Para algunos efectos, esta película de moléculas superficiales se comporta en forma similar a una membrana elástica tirante (la goma de un globo, por ejemplo). De este modo, es la tensión superficial la que cierra una gota y es capaz de sostenerla contra la gravedad mientras cuelga desde un gotario. Ella explica también la formación de burbujas.
La tensión superficial se define en general como la fuerza que hace la superficie (la "goma" que se menciona antes") dividida por la longitud del borde de esa superficie (OJO: no es fuerza dividida por el área de la superficie, sino dividida por la longitud del perímetro de esa superficie). Por ejemplo,
donde F es la fuerza que debe hacerse para "sujetar" una superficie de ancho l. El factor 2 en la ecuación se debe a que una superficie tiene dos "áreas" (una por cada lado de la superficie), por lo que la tensión superficial actúa doblemente.
Algunos valores de la tensión superficial son:
La siguiente figura muestra un ejemplo de cómo algunos animales utilizan la tensión superficial del agua. En la figura se observa un arácnido, fotografiado mientras camina sobre el agua. Se observa que el peso del arácnido está distribuido entre sus ocho patas y el abdomen, por lo que la fuerza de sustentación que debe proveer la superficie del agua (la tensión superficial) sobre las ocho patas y el abdomen debe ser igual al peso del arácnido.
| |||||||||||||||||||||
10-14
|
MAYO
| ||||||||||||||||||||||
16-21
|
MAYO
|
Principio Alquimides
| |||||||||||||||||||||
23-28
|
MAYO
|
Electricidad y Magnetismo
| |||||||||||||||||||||
31-4
|
MAYO-JUNIO
|
Metales y Electrones
| |||||||||||||||||||||
13-18
|
JUNIO
|
Interacción electrica
| |||||||||||||||||||||
20-25
|
JUNIO
|
Corriente electrica
| |||||||||||||||||||||
27-2
|
JUNIO-JULIO
|
Relación entre calor y la electricidad
| |||||||||||||||||||||
5-9
|
JULIO
|
Imanes y polos Magnéticos
|
11-16
|
JULIO-
|
Calor y electricidad
|
18
|
JULIO
|



 Este coeficiente es característico de cada material y se mide en K-1 en unidades del S.I.
Este coeficiente es característico de cada material y se mide en K-1 en unidades del S.I.









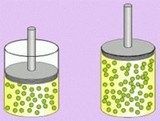
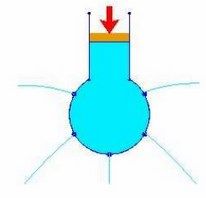
La presión en todo el fluido es constante: esta frase que resume de forma tan breve y concisa la ley de Pascal da por supuesto que el fluido está encerrado en algún recipiente, que el fluido es incompresible... El principio de Pascal puede comprobarse utilizando una esfera hueca, perforada en diferentes lugares y provista de un émbolo. Al llenar la esfera con agua y ejercer presión sobre ella mediante el émbolo, se observa que el agua sale por todos los agujeros con la misma presión.
También podemos ver aplicaciones del principio de Pascal en las prensas hidraulicas.
APLICACION DE PRINCIPIO DE PASCAL
El principio de Pascal puede ser interpretado como una consecuencia de la ecuación fundamental de la hidrostática y del carácter altamente incompresible de los liquidos. En esta clase de fluidos la densidad es prácticamente constante, de modo que de acuerdo con la ecuación:Donde:
Si se aumenta la presión sobre la superficie libre, por ejemplo, la presión total en el fondo ha de aumentar en la misma medida, ya que el término ρgh no varía al no hacerlo la presión total (obviamente si el fluido fuera compresible, la densidad del fluido respondería a los cambios de presión y el principio de Pascal no podría cumplirse)
PRENSA HIDRAULICA
La prensa hidráulica es una máquina compleja semejante a un camión de Arquímides, que permite amplificar la intensidad de las fuerzas y constituye el fundamento de elevadores, prensas, frenos y muchos otros dispositivos hidráulicos de maquinaria industrial.
La prensa hidráulica constituye la aplicación fundamental del principio de Pascal y también un dispositivo que permite entender mejor su significado. Consiste, en esencia, en dos cilindros de diferente sección comunicados entre sí, y cuyo interior está completamente lleno de un líquido que puede ser agua o aceite. Dos émbolos de secciones diferentes se ajustan, respectivamente, en cada uno de los dos cilindros, de modo que estén en contacto con el líquido. Cuando sobre el émbolo de menor sección S1 se ejerce una fuerza F1 la presión p1 que se origina en el líquido en contacto con él se transmite íntegramente y de forma (casi) instantánea a todo el resto del líquido. Por el principio de Pascal esta presión será igual a la presión p2 que ejerce el fluido en la sección S2, es decir:
con lo que, las fuerzas fueron siendo, siendo S1 < S2 :
y por tanto, la relación entre las fuerza resultante en el émbolo grande cuando se aplica una fuerza menor en el émbolo pequeño será tanto mayor cuanto mayor sea la relación entre las secciones: